
Redoxreacties
De elektronen op de buitenste schil noemen we de valentie-elektronen. Een atoom kan maximum 8 valentie-elektronen hebben. Hiervoor zal het elektronen moeten opnemen of afgeven.
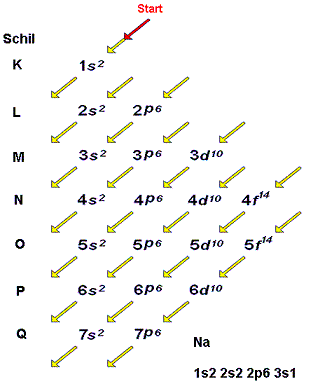
Koolstofatoom
Een redoxreactie is een reactie tussen minstens 2 atoomsoorten waarbij de elektronenwolk verandert. Met andere woorden, een redoxreactie is een reactie waarbij een elektronenoverdracht plaatsvindt van de ene stof naar de andere stof.
Dit kan tussen:
- een metaal en een niet-metaal
- een metaal en een metaal (zie verder: spanningsreeks)
- een niet-metaal en een niet-metaal (zie verder: spanningsreeks)
Een redoxreactie kunnen we opsplitsen in 2 halfreacties waarbij de ene stof elektronen afgeeft (de reductor) en de andere stof elektronen opneemt (de oxidator).
- De halfreactie waarbij de stof elektronen (de reductor) afgeeft, noemen we de oxidatie
- De halfreactie waarbij de stof elektronen (de oxidator) opneemt, noemen we de reductie.
- A) tussen een metaal en een niet-metaal
- vb: De reactie tussen magnesium en zuurstof
-
Mg O2 Elektronenstructuur: K: 2, L: 8, M: 2 Elektronenstructuur: K: 2, L: 6 Mg (reductor) geeft twee elektronen af: oxidatie O (oxidator) neemt twee elektronen op: reductie Halfreactie 1: Mg -> Mg2+ + 2e- Halfreactie 2: O + 2e- -> O2- Magesium wordt geoxideerd (stijgt in OT) Zuurstof wordt gereduceerd (daalt in OT) Het element O komt niet als vrij atoom voor in de natuur. Bij het schrijven van redoxreacties waarbij zuurstof gereduceerd wordt, zal dus ook O2 gereduceerd worden. Halfreactie 1: Mg -> Mg2+ + 2e- Halfreactie 2: O2 + 4e- -> 2O2- De twee halfreacties kunnen we dus schrijven als: oxidatie: Mg -> Mg2+ + 2e- reductie: O2 + 4e- -> 2O2- Uit de Wet van Lavoisier: Er moeten in beide halfreacties evenveel atomen en elektronen (ionen) voorkomen. We moeten hier dus de oxidatie met 2 vermenigvuldigen: 2 (Mg -> Mg2+ + 2e-) Halfreactie 1 : 2Mg -> 2Mg2+ + 4e- Halfreactie 2 : O2 + 4e- -> 2O2- Redox: 2Mg + O2 -> 2Mg2+ + 2O2- 2Mg2+ + 2O2- gaan een binding aan tot 2MgO Redox: 2Mg + O2 -> 2MgO
-
- vb: De reactie tussen magnesium en zuurstof
- Opmerkingen:
- Volgende elementen komen steeds in moleculevorm voor in de vrije natuur: zuurstof (O2), stikstof (N2), fluor (F2), chloor (Cl2), broom (Br2), jood (I2), astaat (At2) en waterstof (H2)
- De stof die de elektronen levert via de oxidatie, noemen we ook de reductor
- De stof die de elektronen opneemt via de reductie, noemen we ook de oxidator
- Het oxidatiegetal van een element wordt door een Romeins cijfer weergegeven, voorafgegaan door een +teken of een -teken
- Rekenregels om het oxidatiegetal te bepalen:
- het oxidatiegetal van een
vrij element is gelijk aan nul
- bv: Mg Mg0
- het oxidatiegetal van een
éénatomig ion is gelijk aan zijn lading
- bv: Na+ Na+I
- Het oxidatiegetal van de alkalimetalen (groep 1a) is +I in alle verbindingen: Na, K, Li, Cs
- Het oxidatiegetal van de aardalkalimetalen is +II in alle verbindingen: Ba, Mg, Be, Sr
- Het oxidatiegetal van waterstof is altijd +I (behalve in metaalhydriden = verbindingen tussen waterstof en een metaal uit groep 1a,2a en 3a => -I)
- Het oxidatiegetal van zuurstof is altijd -II in alle verbindingen (behalve in de peroxiden: -I)
- De som van de
oxidatiegetallen van alle atomen in een neutraal molecuul is
altijd gelijk aan nul
- bv: MgO +II -II = 0
- Aan de atomen in moleculen met een atoombinding (covalente binding)
kan men ook een oxidatiegetal toekennen. We rekenen de bindingselektronen
dan aan bij het element met de hoogste EN-waarde
- bv: CO2
- ENO > ENC => de bindingselektronen horen bij zuurstof
- C = +IV en O = -II(x2)
- In geval van gelijke EN-waarde
(bv: N2) moeten de gemeenschappelijke elektronen gelijk verdeeld
worden:
- :N ... ... N:
- De 6 elektronen van de drievoudige covalente binding worden gelijk verdeeld over de 2 stikstofatomen. Hierdoor krijgen ze 5 valentie-elektronen zoals in de neutrale atomaire toestand. Het OG van N is gelijk aan nul
- bv: CO2
- De som van de oxidatiegetallen van alle atomen in een ion is gelijk
aan de lading van het ion
- NO3- : N: +V en O: -II(x3) => +V - VI = -I
- B) tussen een metaal en een metaal
- Verdringingsreeks of spanningsreeks van de metalen
- Metalen (hebben de neiging elektronen af te geven = reductoren: ze hebben een lage EN-waarde <1,5)
- Rangschikking van de metalen volgens opklimmende
elektronegativiteit
- Li - K - Ba - Ca - Na - Mg - Al - Zn - Fe - Ni - Pb - H2 - Cu - Hg - Ag - Pt - Au
- lichte metalen (zeer onedel) -
onedele metalen - halfedele metalen -
edele metalen
- De lichte metalen hebben een kleine elektronegativiteit (EN-waarde). Ze zullen hun elektronen makkelijk afstaan (geoxideerd worden). Ze reageren zelfs met water: (H2O -> H+ + OH-)
-
oxidatie: 2 Na -> 2 Na+ + 2e- reductie: 2 H+ + 2e- -> H2↑ redox: 2 Na + 2H+ + 2 OH- -> 2 Na+ + H2↑ + 2 OH- - De onedele metalen hebben een hogere EN-waarde dan de zeer onedele metalen en staan hun buitenste elektronen minder makkelijk af. Ze reageren zeer traag met water.
- De halfedele en de edele metalen hebben een nog grotere EN-waarde en reageren zeer traag tot niet met water.
- Bij een reactie tussen 2 metalen (één
in vaste vorm en één in ionvorm) zal het onedeler metaal
geoxideerd
worden (elektronen afstaan) door de metaalionen die hoger in de
spanningsreeks staan en die een hogere EN-waarde hebben. Ieder metaal kan
dus een ion van het metaal dat rechts van hem staat oxideren. Het onedeler
metaal zal dus steeds zijn elektronen afgeven aan een edeler metaalion:
- bv: Zink en kopersulfaat: Kan men een kopersulfaat-oplossing ( CuSO4 -> Cu2+ + SO42- ) in een vat van zink ( Zn ) bewaren?
- Zink is onedeler dan koper en houdt zijn elektronen niet erg sterk vast. Koper staat ook rechts van zink in de spanningsreeks. Wanneer een koperion in de nabijheid van een zinkatoom komt, zal het koperion de buitenelektronen van het zink afnemen: (zink wordt geoxideerd en koper wordt gereduceerd!)
-
oxidatie: Zn -> Zn2+ + 2e- reductie: Cu2+ + 2e- -> Cu↓ redox: Zn + Cu2+ -> Zn2+ + Cu↓ - !!!! Bewaar dus nooit een kopersulfaatoplossing in een zinken vat want het zal in oplossing gaan !!!
- bv: Koper en ijzersulfaat: Kan men een ijzersulfaat-oplossing ( FeSO4 -> Fe2+ + SO42- ) in een koperen vat bewaren?
- Koper is edeler dan ijzer en houdt zijn elektronen stevig vast! Ijzer staat links van koper in de spanningsreeks. Wanneer een ijzerion in de buurt van een koperatoom komt, zal het ijzerion de buitenelektronen van het koper niet kunnen afnemen! (koper wordt niet geoxideerd en ijzer wordt niet gereduceerd!)
- Er vindt dus geen redoxreactie plaats en men kan dus een ijzersulfaat-oplossing in een koperen vat bewaren!
- bv: Koper en diwaterstofsulfaat: Kan men een diwaterstofsulfaat-oplossing ( H2SO4 -> 2H2+ + SO42- ) in een koperen vat bewaren?
- Waterstof staat links van koper in de spanningsreeks. Wanneer een waterstofion in de buurt van een koperatoom komt, zal het waterstofion de buitenelektronen van het koper niet kunnen afnemen! (koper wordt niet geoxideerd en waterstof wordt niet gereduceerd!)
- Maar: H2SO4 + Cu -> CuO + H2O + SO2↑
- C) tussen een niet-metaal en een niet-metaal
- Verdringingsreeks of spanningsreeks van de niet-metalen
- Niet-metalen (hebben de neiging elektronen op te nemen = oxidatoren: ze hebben een hoge EN-waarde >2,5)
- Rangschikking van de niet-metalen volgens dalende
elektronegativiteit
- F2 - O2 - Cl2 - Br2 - I2 - S
- Fluor is een zeer sterke oxidator en zwavel is een zwakke oxidator. De sterke niet-metalen geven dus hun elektronen minder makkelijk af! Ze nemen ze wel sneller op!! Ieder niet-metaal kan het niet-metaalion rechts van hem oxideren! Chloor is een sterkere oxidator (neemt makkelijk elektronen op en heeft dus een hogere EN-waarde) dan broom. Broom is een zwakkere oxidator dan chloor en zal dus zijn elektronen aan een choorion afstaan.
- Vb. 1: Wanneer chloorgas ( Cl2 ) door een natriumbromide-oplossing ( NaBr -> Na+ + Br- ) geleid wordt, zal chloor het bromide-ion oxideren tot broom (of het bromide-ion zal chloor reduceren tot chloride):
-
oxidatie: 2 Br- -> Br2 + 2e- reductie: Cl2 + 2e- -> 2Cl- redox: 2Br- + Cl2 -> Br2 + 2Cl- - Vb. 2: Kan broom ( Br2 ) geleid door een natriumchloride-oplossing ( NaCl -> Na+ + Cl- ) de chloride-ionen oxideren tot chloor? Broom staat in de spanningsreeks rechts van chloor. Broom houdt zijn elektronen steviger vast dan chloor met als gevolg dat het leiden van broomgas door een chlorideoplossing geen oxidatie tot gevolg heeft!
- Uit de twee bovenstaande voorbeelden maak je dus op dat de niet-metalen de niet-metalen rechts van zichzelf kunnen oxideren en niet omgekeerd!
| Aluminium en zwavel | metaal en niet-metaal |
| 2 (Al -> Al3+ + 3e-) (oxidatie door reductor Al) | 3(S + 2e- -> S2-) (reductie door oxidator S) |
| redox: 2Al + 3S + 6e- -> 2Al3+ + 3S2- + 6e- (6e- mag je schrappen links en rechts) | |
| redox: 2Al + 3S -> Al2S3 | |
| Zink en chloor | |
| Zn -> Zn2+ + 2e- (oxidatie door reductor Zn) | Cl2 + 2e- -> 2Cl- (reductie door oxidator Cl2) |
| redox: Zn + Cl2 + 2e- -> Zn2+ + 2Cl- + 2e- (2e- mag je schrappen links en rechts) | |
| redox: Zn + Cl2 -> ZnCl2 | |
| Kalium en broom | metaal en niet-metaal |
| 2 (K -> K+ + 1e-) | Br2 + 2e- -> 2Br- |
| redox: 2K + Br2 + 2e- -> 2KBr + 2e- | |
| redox: 2K + Br2 -> 2KBr | |
| Zoutzuur en magnesium | metaal en metaal |
| 2H+ + 2e- + 2Cl- -> H2↑ + 2 Cl- (reductie) | Mg -> Mg2+ + 2e- (oxidatie) |
| redox: 2H+ + 2e- + 2Cl- + Mg -> H2↑ + 2 Cl- + Mg2+ + 2e- | |
| redox: 2H+ + 2Cl- + Mg -> H2↑ + 2 Cl- + Mg2+ | |